2일 글로벌경제신문 단독 보도에 의하면 식품의약품안전처(처장 이의경)는 지난달 31일 ‘인보사케이주’(유전자치료제)의 주성분 중 1개 성분(2액)이 허가 당시 제출한 자료에 기재된 연골세포와 다른 신장세포주인 것으로 추정돼 코오롱생명과학에 제조·판매중지를 요청한 것으로 전해졌다.
글로벌경제신문에 따르면 인보사케이주의 유전자 세포주 성분의 구축 과정인 최초 연구개발은 코오롱생명과학 미국 바이오법인 코오롱티슈진이 주도했는데 유전자치료제에 필요한 세포를 이용하기 위해서는 단일세포주를 배양해야만 한다.
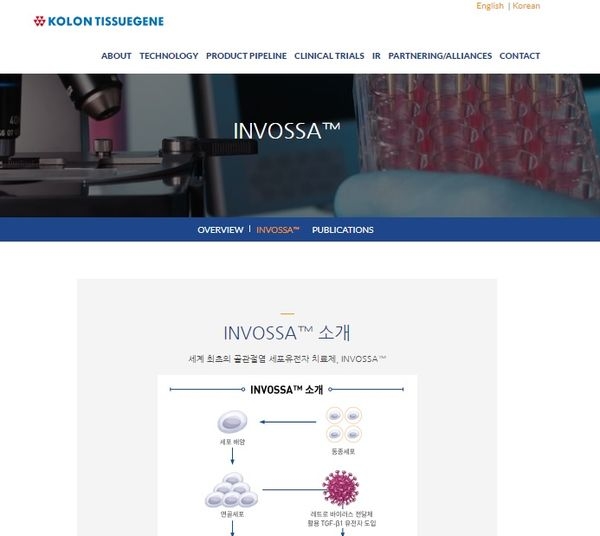
유전자치료제에 사용될 최초 단일세포를 배양하기 위해서는 리서치셀뱅크(Research Cell Bank)가 필요하며 이 단계에서 연구가 주로 이루어진다.
세포의 특성이 확립된 후 마스터셀뱅크(Master Cell Bank)를 만들어 의약품에 사용하는 원료를 얻을 수 있는데 유전자치료제의 최종단계는 마스터셀뱅크에서 세포를 꺼내 사용하는 데 한계가 있어 더 많이 배양해 만드는 것이 워킹셀뱅크(Working Cell Bank)이다.
코오롱생명과학 측은 왜 세포가 바뀌었느냐는 식약처의 질문에 대해 처음부터 바뀌었는데 그 사실을 몰랐다고 밝힌 것으로 전해졌다. 이에 대해 식약처는 연구단계인 리서치셀뱅크에서 세포가 바뀔수는 있어도 마스터셀뱅크와 워킹셀뱅크가 바뀔 수 없다고 추정하고 이를 확인 중이다.
매체에 따르면 결국은 처음 세포가 구축되는 배양시기부터 잘못된 것인데 식약처와 코오롱생명과학이 제대로 확인하지 못했다는 결론이다.
이와 관련 식약처 관계자는 유전자 치료제의 경우 형질변환이 된다 보니 승인 당시에는 세포주 확인에 필요한 유전자 검사를 할 수 없었고 코오롱생명과학이 제출한 자료를 확인 및 검증해 결론을 내리게 됐다고 밝혔다.
한편 식약처에 따르면 인보사케이주 해당 제품이 납품되고 있는 병·의원은 443개소이며, 유전자치료제 투약 가능 병··의원은 총 912개소이며 해당 제품 이외에 골관절염 치료제로 오랫동안 시술돼 왔다. 또 1회 시술에 700만원을 호가했지만 비수술적 치료이기에 골관절염 초기 및 중기 단계의 환자들에게 인기리에 시술돼왔다.
업계에 따르면 병원은 약품의 효능을 믿고 치료했기에 해당 시술을 받은 환자의 경우 개인적인 효과 및 효능은 다르겠지만 코오롱생명과학에는 손해배상을 청구할 수가 있다는 견해를 제시하고 있다.
한편 코오롱생명과학은 "인보사의 안전성과 유효성에 문제가 없어 허가취소에 해당하지 않는다"고 주장하고 있지만, 규제당국인 식품의약품안전처는 "업체의 고의 여부에 대해 면밀히 조사한 결과에 따라 결정하겠다"는 입장이여서 허가 취소 가능성도 열려있는 상황이라는게 이 매체의 지적이다.
news@thebigdata.co.kr
<저작권자 © 빅데이터뉴스, 무단 전재 및 재배포 금지>